
麻省理工學院(MIT)工程師們開發出一種復制神經肌肉接頭(神經和肌肉之間至關重要的連接)的微流控設備(microfluidic device)。該設備約有25美分硬幣大小,包含單個肌條和一小組運動神經元。研究人員能夠在逼真(現實)的三維基質中影響和觀察兩者之間的相互作用。
研究人員對該設備中的神經元進行基因改造,使其對光照做出反應。通過將光照投射到(這些)神經元上,能夠精確刺激這些細胞,發送信號激發肌肉纖維。研究人員還測量了設備內肌肉在被激發后抽搐或收縮的力量。
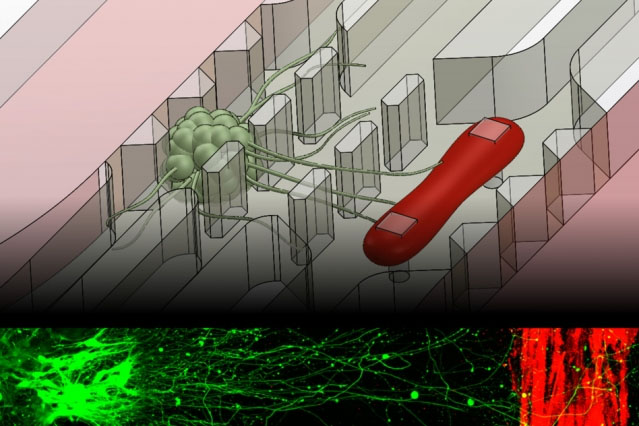
復制神經肌肉接頭的新型微流控設備。該設備包含一小群簇神經元(綠色)和單個肌肉纖維(紅色)。
下方的熒光圖像顯示了運動神經元跨越約1毫米的距離向肌條發出軸突。
研究結果2016年8月3日在線發表于《Science Advances》期刊,可能幫助科學家們理解并識別藥物以治療肌萎縮側索硬化(ALS,即盧伽雷氏癥)和其他神經肌肉相關疾病。
“神經肌肉接頭涉及許多失能性疾病,其中有些是殘酷而致命的,還有很多尚未被發現”領導該研究的MIT機械工程系研究生SebastienUzel說,“我們希望能夠在體外形成神經肌肉接頭,從而幫助我們理解某些疾病活動”。Sebastien Uzel現在是哈佛大學Wyss研究所博士后。

自1970年代以來,科學家們已經提出了大量方法在實驗室中模擬神經肌肉接頭。這些實驗大部分涉及在培養皿或小玻璃基板上生長肌肉和神經細胞。但這樣的環境與(動物)體內狀態相去甚遠,在動物體內,肌肉和神經細胞存活于復雜的三維環境中,并且通常距離較遠。
“想想長頸鹿”Uzel說,“脊髓神經元所發出的軸突需要跨越非常大的距離才能與腿部肌肉連接。”
為了在體外重建更逼真的神經肌肉接頭,Uzel和同事們構造了一種微流控設備,該設備具有兩個重要特性:1. 三維環境;2. 隔離肌肉和神經的隔間,從而模擬兩者在人體內的自然分離狀態。研究人員將肌肉和神經元細胞懸浮于隔間中,然后充滿凝膠以模擬三維環境。
為了生長肌肉纖維,研究團隊使用了獲得自小鼠的肌肉前體細胞,隨后將其分化成肌肉細胞。他們將細胞注入微流控隔間,細胞會在隔間內生長并融合形成單個肌條。同樣的,他們從干細胞分化出運動神經元,然后將所獲得的神經細胞聚合體放置在第二個隔間中。在分化兩種細胞之前,研究人員使用光遺傳學(optogenetics)技術對神經細胞進行了基因改造。
該研究共同作者、MIT機械和生物工程Ceciland Ida Green特聘教授Roger Kamm說:光“能夠讓你精確控制你想要激活的細胞”。在這樣的狹小空間里,電極無法實現這一點。

最后,研究人員為該設備添加了另一個特性:力傳感。為了測量肌肉收縮,他們在肌肉細胞隔間內構造了兩個微小的彈性支柱,位于肌肉纖維周圍并能夠被生長的肌肉纖維所包裹。隨著肌肉收縮,支柱會被擠壓在一起,形成位移,研究人員能夠測量這些位移并轉換為機械力。

研究人員構造的微流控設備。將肌肉和神經元細胞懸浮于水凝膠,并注入到毫米尺寸的隔間中(藍色細通道),隨后從神經元/肌肉組織兩側分別提供培養基(藍色大通道),模擬三維環境。
在測試該設備的實驗中,Uzel和同事們首次觀察到神經元在三維區域內向肌肉纖維伸展軸突。在觀察到軸突建立連接時,他們用微小的藍光激射刺激神經元,并立即觀察到肌肉收縮。
“發射閃光,就能觀察到抽搐”Kamm說道。
根據這些實驗,Kamm說,這種微流控設備可能作為神經肌病藥物測試卓有成效的試驗場,甚至可以根據個體患者進行定制。
“你可能從ALS患者獲得多能細胞,將它們分化成肌肉和神經細胞,并且為特定患者制造整個系統”Kamm說,“然后你能夠根據需要多次復制,同時測試不同的藥物或療法的組合,查看哪種療法能夠最有效地改善神經和肌肉之間的連接。”
另一方面,他說,該設備在“建模操作協議(modeling exercise protocols)”中可能是有用的。例如,通過以不同的頻率刺激肌肉纖維,科學家們能夠研究重復壓力如何影響肌肉的性能。
“現在,隨著所有這些新型微流控方法的開發,你能夠開始建立神經元和肌肉的更復雜的模型”Kamm說,“神經肌肉接頭是另一個現在可以被納入測試模式的單位”。